Farmaci anti-obesità, una volta sospesi si riprende il 60% del peso
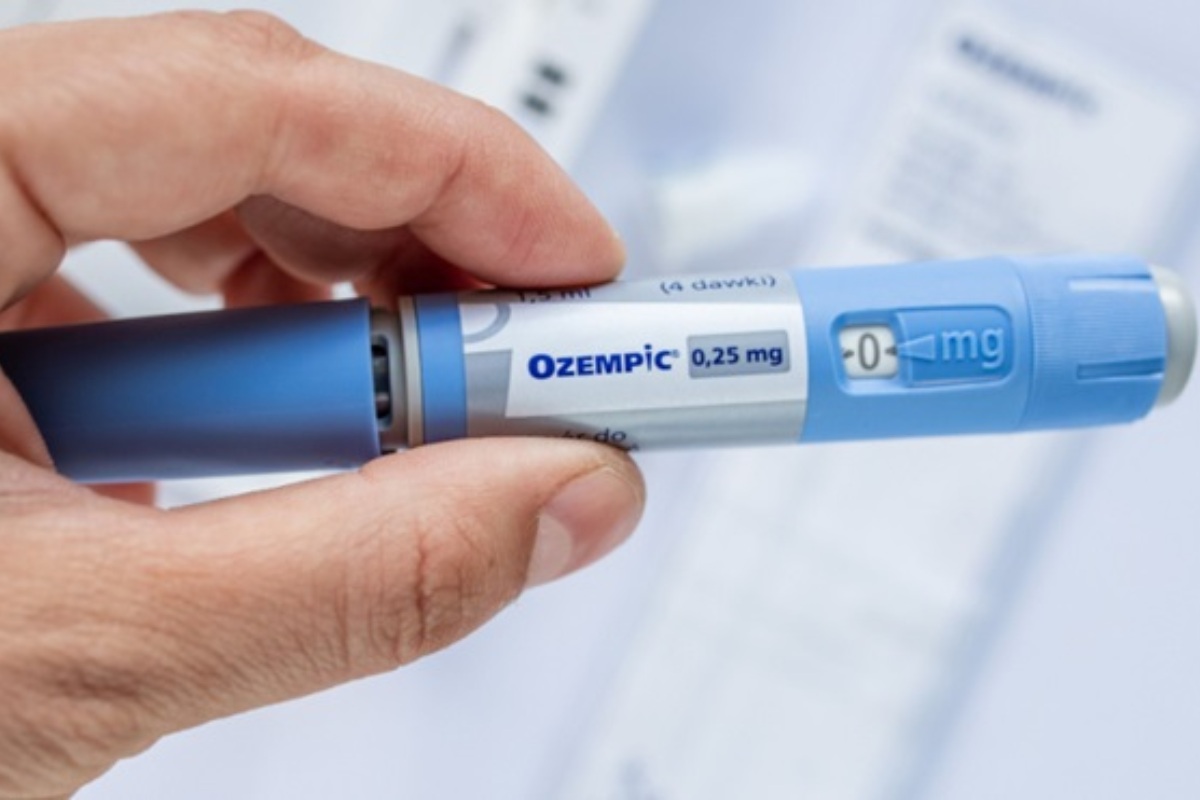

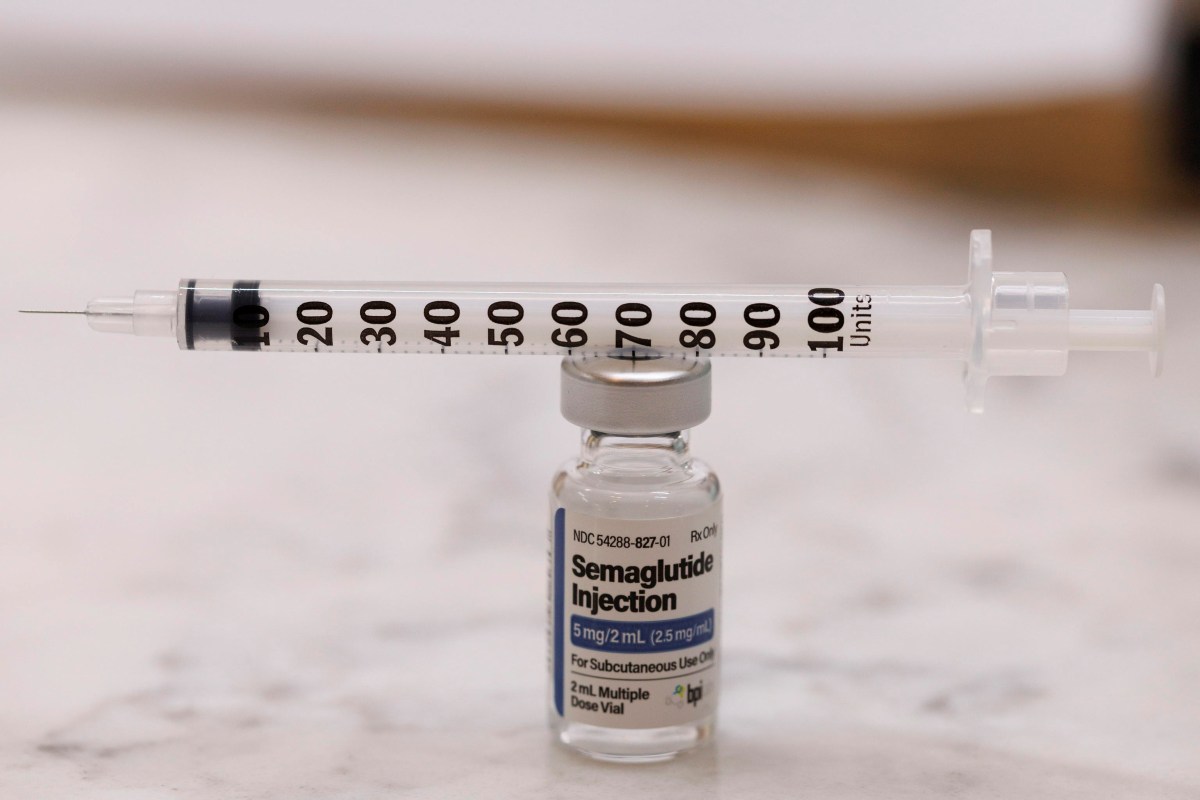
Il dimagrimento ottenuto assumendo i farmaci anti-obesità della classe degli agonisti del recettore Glp-1 – di cui fa parte la categoria più nota dei semaglutide come Ozempic – non dura a lungo una volta sospesa la terapia. I pazienti che interrompono il trattamento riprendono il 60% dei chili eliminati. Il nuovo aumento di peso arriva entro un anno dalla fine della terapia. A sostenerlo è il report di un team di ricercatori dell’università di Cambridge pubblicato sul Journal eClinicalMedicine.
Ozempic, Wegovy, Rybelsus e tirzepatide.
L’analisi riguarda i dati emersi in 48 studi sugli effetti a medio termine di prodotti come Ozempic, Wegovy, Rybelsus e tirzepatide. Il rapporto ha inoltre messo a punto proiezioni statistiche sugli effetti a più lungo termine della sospensione delle cure con i farmaci contro l’obesità. Secondo gli studiosi, nel tempo i pazienti hanno alte probabilità di riacquistare addirittura il 75% del peso inizialmente eliminato. Alcuni esperti osservano però che l’uso di questi medicinali appare capace di mantenere una diminuzione di almeno il 5% del peso iniziale dei pazienti. Una percentuale comunque significativa.
Le morti
Intanto la Food and drug administration americana (Fda) ha mandato una lettera di richiamo a Novo Nordisk, l’azienda che ha messo a punto i farmaci Ozempic e Wegovy. Tre persone che stavano prendendo rispettivamente uno dei due medicinali sono morte. Una è deceduta per suicidio. Il legame di causa ed effetto non è provato. Ma la Fda cita gravi violazioni da parte della Novo Nordisk per non aver riportato le morti alla stessa agenzia Usa che controlla appunto la sicurezza dei farmaci. E per non avere avviato alcuna investigazione sulla possibilità che i decessi fossero in qualche modo legati ad effetti collaterali dei prodotti semaglutide.
Ti potrebbe interessare
- Obesità, una malattia anche per la legge: Italia prima nel mondo ma cosa cambia davvero e a quali cure si può accedere?
- La rivelazione della senatrice Michaela Biancofiore: «Assumo il farmaco per dimagrire, ho perso 17 chili, ma ora ho lo stesso problema di Robbie Williams»
- Semaglutide e Ozempic: la moda semiclandestina delle punture per dimagrire
La lettera
Nella lettera datata 5 marzo, la agenzia governativa ricorda: «La nostra attività di verifica della sicurezza dei medicinali in commercio e per la protezione della salute pubblica si basa proprio sul dovere delle aziende di notificare eventuali eventi avversi registrati nei fruitori dei farmaci», La Fda ha dato due settimane di tempo a Novo Nordisk per spiegare l’accaduto ed illustrare le azioni che intende mettere in atto per evitare future violazioni.