Vaccini, Moderna chiede all’Ema il via libera per la terza dose: «Risposta significativa contro la variante Delta»
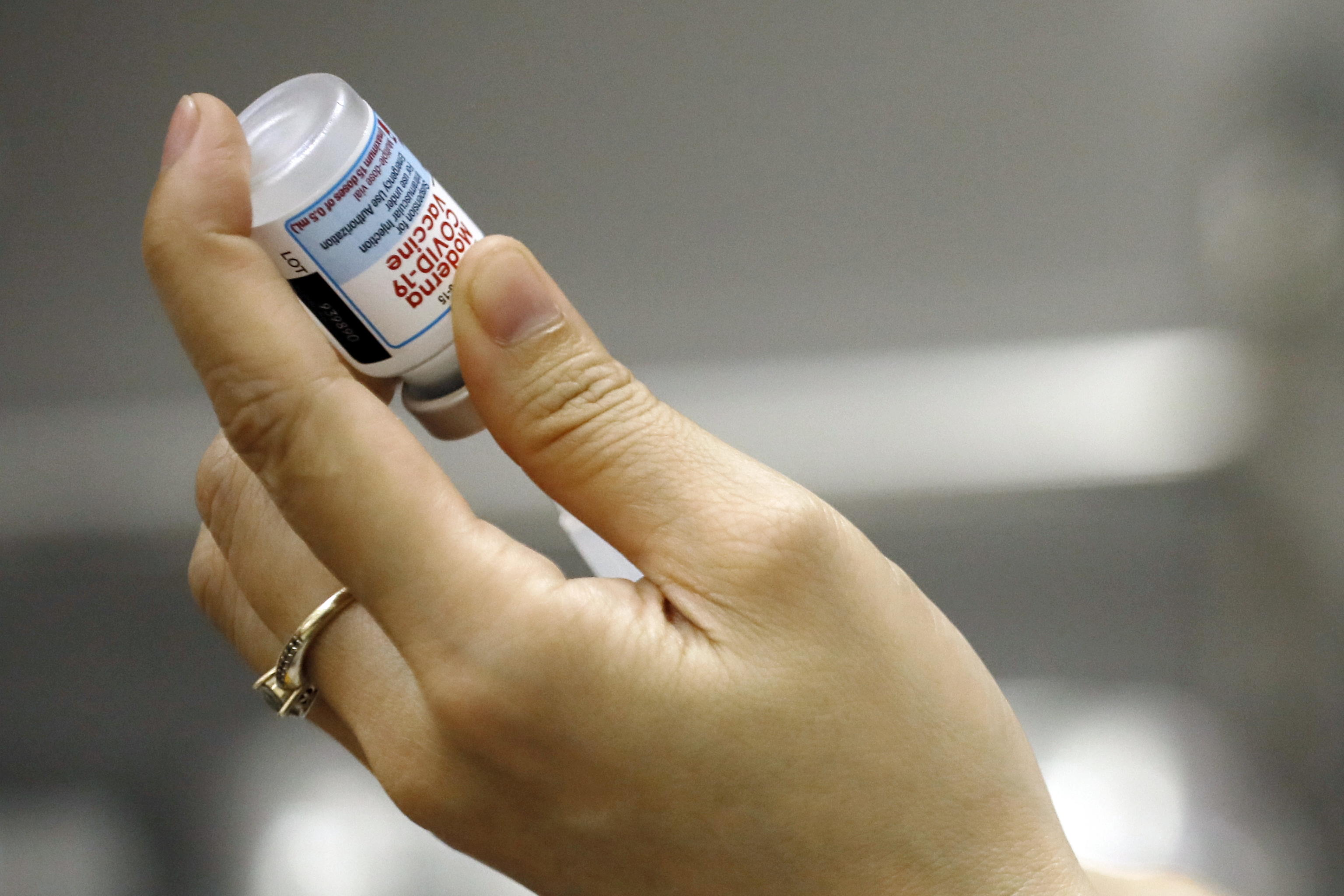

L’azienda farmaceutica Moderna ha presentato all’Agenzia europea per i medicinali (Ema) i dati per chiedere l’approvazione per la somministrazione della terza dose del vaccino anti-Coronavirus. A darne notizia è la stessa società statunitense che ha diffuso una nota. Moderna aveva già presentato la richiesta alla Food and Drug Administration, l’ente di regolamentazione farmaceutica statunitense, che dovrebbe esprimersi a riguardo nel giro di pochi giorni. L’amministratore delegato Stéphane Bancel ha spiegato che, secondo quanto emerso dagli studi di Fase 2, una dose di richiamo di 50 microgrammi del vaccino induce «robuste risposte anticorpali contro la variante Delta». A circa 6 mesi dalla seconda dose, quando la protezione diminuisce, si è osservato che il richiamo di mRNA-1273 «aumenta significativamente i titoli anticorpali neutralizzanti». L’effetto positivo si è riscontrato in pazienti di tutte le età, in particolare negli anziani di età pari o superiore a 65 anni. Ma la buona notizia non riguarda solo la lotta alla variante Delta: un’analisi aggiuntiva ha mostrato che una dose di richiamo di mRNA-1273 ha indotto risposte anticorpali robuste e un aumento dei titoli anticorpali per tutte le varianti di interesse, tra cui Beta (B.1.351) di 32 volte, Gamma (P.1) di 43,6 volte e Delta (B.1.617.2) di 42,3 volte. Per il momento non è ancora stata definita la posizione dell’Ema riguardo alla necessità o meno di pensare una terza dose.
Immagine di copertina: EPA/LUONG THAI LINH
Leggi anche:
- «I vaccini per i bambini in arrivo a novembre, saranno Pfizer e Moderna»: l’annuncio di Locatelli (Cts)
- Miocardite e vaccini a mRNA, Ema: infiammazioni al cuore molto rare dopo Pfizer e Moderna. Perché restano «sicuri»
- Pfizer e Moderna aumentano i prezzi dei vaccini all’Ue: 19,5 euro e 25,5 dollari a dose per la fornitura fino al 2023
- Vaccini, la conferma dell’Oms: la doppia dose di AstraZeneca è meno efficace del mix con Pfizer o Moderna
- Vaccini, Israele autorizza la terza dose di Pfizer per gli over 60: è il primo Paese al mondo

