No! Un documento AIFA non rivela che i vaccini non sono stati sperimentati in doppio cieco


Sta circolando in diverse condivisioni Facebook (per esempio qui e qui) lo screen di un documento Aifa dove sembrerebbe che i vaccini contro il nuovo Coronavirus siano stati approvati mediante semplici verifiche in cieco (non in doppio cieco) e che quindi gli sperimentatori avessero saputo fin da subito a quali pazienti somministravano il farmaco o il placebo. Questo genere di post sembrano sollevare una obiezione acuta e sacrosanta, ma solo se si evita di risalire al documento nella sua interezza e allo studio a cui fa riferimento; altrimenti questo genere di narrazioni si rivelerebbero subito infondate. Vediamo perché.
Per chi ha fretta:
- Il documento di Aifa in oggetto definisce i termini entro cui monitorare i volontari dello studio di terza fase di Johnson & Johnson sul suo vaccino Covid.
- Lo studio in sé, come indicato dalle fonti fornite dalla stessa Agenzia, è stato svolto inequivocabilmente in doppio-cieco.
Analisi
La narrazione – probabilmente derivata da una serie di tweet pubblicati dalla utente BlackWitch il 21 dicembre 2022 -, è la seguente:
Questa è la riprova ufficiale e fondamente del marcio che sta nella medicina. La vaccinazione, non è stata fatta a doppio cieco, ma a CIECO. E di qui viene fuori un fatto fondamentale i medici vaccinatori SAPEVANO a chi davano il placebo e a chi il vaccino. È per questo che hanno fatto tutto il casino sul green pass, e sulle vaccinazioni.
L’ UNICO MODO PER RESTITUIRE i dati a chi stava facendo questa sperimentazione, non di un vaccino, ma di una medicina.Era il green pass.
Questo è stato un trial e questo è il documento ufficiale che lo dimostra, questo non è un vaccino, ma bensì una medicina sperimentata sulla pelle dei poveri cristi che se lo sono fatto…
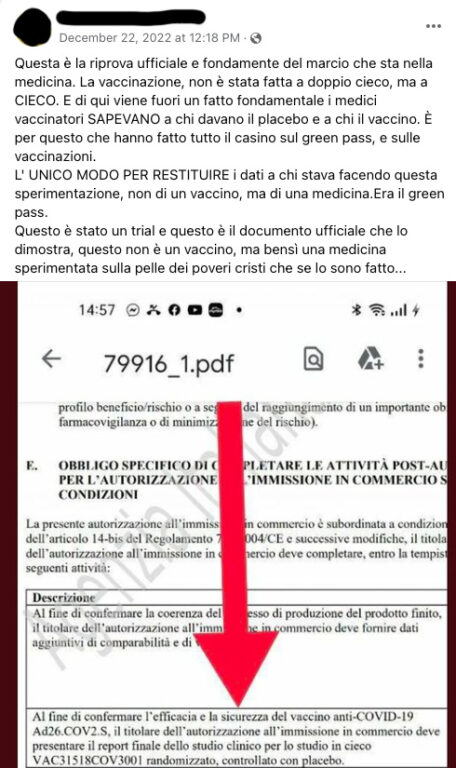
In cima allo screen abbiamo il nome del file: 79916_1.pdf, reperibile in Rete (qui, pag. 19). Si parla di Ad26.COV2.S, ovvero del vaccino di Johnson & Johnson. «Il titolare dell’autorizzazione all’immissione in commercio deve presentare il report finale dello studio clinico per lo studio in cieco VAC31518COV3001 randomizzato, controllato con placebo». La data di “scadenza” indicata è «31 dicembre 2023». Abbiamo dunque anche il codice di riferimento che ci permette di reperire il trial, qui e qui. Nella seconda fonte è più facile notare che il contesto è quello di un esperimento clinico di terza fase «double-blind», ovvero in doppio cieco:
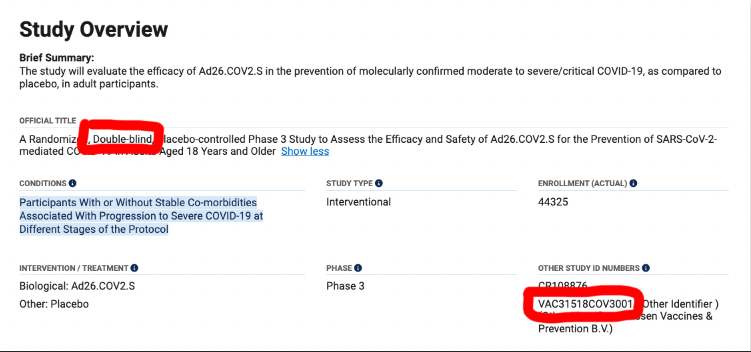
Una spiegazione del contesto a cui fa riferimento il documento di Aifa (per altro derivata da un contesto differente), la troviamo nel lavoro dei colleghi di Reuters e Facta, in risposta a chi chiedeva «di verificare se i vaccini prodotti abbiano realmente raggiunto la cosiddetta ‘Fase 4’ di sperimentazione, dal momento che “lo studio in fase 3 finisce nel 2023″». La Fase 3, quella descritta nello studio «double-blind», si è conclusa per tutti i vaccini approvati da Aifa, quindi anche dall’Ema. Ma le case farmaceutiche devono sempre monitorare i volontari che hanno partecipato al trial, proprio perché, con buona pace dei No vax, si continua sempre a vigilare su eventuali eventi avversi, anche se palesemente i benefici della vaccinazione superano di misura i presunti quanto rari rischi.
Conclusioni
Le indicazioni di Aifa riguardo al continuo monitoraggio dei volontari che hanno partecipato al trial di Johnson & Johnson per il suo vaccino Covid, sono state confuse con le condizioni in cui si è svolto lo studio in oggetto, ch’è presentato inequivocabilmente in doppio-cieco. Si tratta di documenti di una Agenzia governativa rivolti alle case farmaceutiche, per tanto risultano poco chiari a un pubblico più vasto.
Questo articolo contribuisce a un progetto di Facebook per combattere le notizie false e la disinformazione nelle sue piattaforme social. Leggi qui per maggiori informazioni sulla nostra partnership con Facebook.
Leggi anche:
- Spoils system all’Aifa: Nicola Magrini non sarà più il direttore generale
- «La campagna di vaccinazione deve proseguire», l’appello di Magrini (Aifa): l’urgenza per fragili con l’incognita Cina
- Covid meno letale dell’influenza? Crisanti durissimo col capo di Aifa Palù: «È analfabetismo: così fa disinformazione in malafede»
- Pressing della autorità sanitarie sui vaccini anti Covid: «Circolazione del virus ora sopra la soglia: serve proteggersi»
- Covid, via libera di Aifa ai vaccini per le nuove varianti Omicron Ba.4 e Ba.5: «Tutti i booster ugualmente efficaci»
